Qué es el CMV

Tengas hijos o no, seguro que has escuchado hablar cientos de veces sobre las precauciones que hay que tener con los gatos durante el embarazo para evitar la toxoplasmosis. O sobre la recomendación de que las futuras madres no coman determinados alimentos, como carne o pescado crudos, huevos sin cocinar o ciertos tipos de queso, por riesgo de listeriosis. Millones de madres de todo el mundo se hacen las pruebas cada año para descartar el síndrome de Down. Pero, ¿y sobre el citomegalovirus (CMV)? ¿Nadie te ha hablado? No en vano lo llaman el “virus silencioso”.
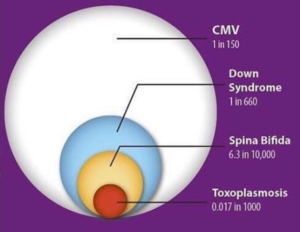
Lamentablemente, muy pocas madres o futuras madres conocen esta enfermedad, pese a que el citomegalovirus congénito es la infección viral de nacimiento más común: uno de cada 150 bebés nace afectado. Hay más niños con discapacidades debido al CMV congénito que por otras causas más conocidas como el Síndrome de Down, el síndrome de alcoholismo fetal, espina bífida o VIH/SIDA pediátrico. En algunos casos, las consecuencias son realmente graves: sordera, ceguera, parálisis cerebral, discapacidad física y mental, convulsiones y muerte.
Y el caso es que el CMV, un virus muy común, de la misma familia del herpes, es realmente fácil de prevenir con la información adecuada y unas sencillas rutinas higiénicas. Y aunque todavía no se ha encontrado una vacuna o una cura, una detección temprana (incluso antes del parto) es clave para frenar el avance de la enfermedad en los niños.
Fuente: CMV Australia
Por eso las asociaciones de familias afectadas de todo el mundo se han propuesto dedicar el mes de junio a divulgar información sobre el Citomegalovirus, sus causas, efectos, prevención y opciones de tratamiento (en España una de las plataformas es @MamasCMV – en Instagram y Twitter – y Stop CMV en la web www.stopcitomegalovirus.org).
En la mayoría de los casos, el CMV es casi inofensivo y las personas sanas que lo contraen no suelen mostrar ningún síntoma. Pero puede transmitirse al feto en el caso de que la madre se infecte algo que se produce con frecuencia por contacto con otros niños de corta edad. De hecho, es conocida como la enfermedad del segundo hijo, porque es común que suceda cuando hay hermanos entre 1-3 años en casa. Eso no significa que el bebé desarrolle automáticamente la enfermedad, pero cuando sucede las consecuencias pueden ser realmente serias.
ES CONOCIDA COMO LA ENFERMEDAD DEL HERMANO MAYOR
El CMV representa así un riesgo importante para las mujeres embarazadas, especialmente las que ya son madres, trabajadoras de guarderías, maestras de preescolar, terapeutas, médicos y enfermeras. El CMV está presente en la saliva, orina, lágrimas, sangre, mocos y otros líquidos corporales. Por eso se recomienda, por ejemplo, que las futuras madres no besen a niños en los labios o no compartan cubiertos con ellos. También que se laven las manos con frecuencia si se ha estado en contacto con pañales u otras secreciones.
Las embarazadas pueden contraer la infección durante el embarazo, y alrededor del 40% transmiten la infección al feto. Algunas infecciones pueden dar fiebre, aumento de los ganglios del cuello, dolor de garganta, o incluso una mononucleosis con afectación de las enzimas del hígado, pero muchas no producen síntomas. La serología rutinaria (detección de anticuerpos frente al virus) durante el embarazo no está recomendada, y solo se hace en algunos centros públicos y privados y por supuesto ante la presencia de síntomas sugestivos en la madre o alteraciones ecográficas del feto.
En las mujeres el diagnóstico de infección se hace por serología (anticuerpos IgM e IgG frente al virus en sangre). Las mujeres con infección presentan IgM positiva, por lo que cualquier mujer con IgM positiva frente a CMV debe consultar con su ginecólogo. Muchas mujeres pueden tener anticuerpos IgG positivos, pero esto solo indica que ya han pasado la infección en algún momento de su vida. Si una mujer presenta IgM positiva e IgG positiva, se debe hacer una prueba que se llama avidez de los anticuerpos IgG. Si la avidez es baja, la infección en la madre ha sido reciente (en los últimos 3 meses). Si la avidez es alta, han pasado más de 6 meses desde que contrajo la infección. Hay casos de avidez intermedia o indeterminada (entre 3-6 meses).
Existe la posibilidad de que una mujer que haya pasado la infección antes de estar embarazada pueda reactivar el virus durante el embarazo y contagiar al feto. En estos casos la transmisión es mucho menos frecuente (1-2% de los casos). El diagnóstico de la madre es muy difícil porque ya tienen anticuerpos previos, aunque en muchas mujeres se positivizan a títulos bajos los anticuerpos IgM.
La transmisión madre-hijo es menos frecuente si la infección se produce en el primer trimestre y más alta en infecciones en el tercer trimestre. Sin embargo, la gravedad (posibilidad de que el niño nazca con síntomas de la infección) es más alta si se produce transmisión en el primer trimestre y mucho menor en las infecciones del tercer trimestre.

En una mujer con infección demostrada durante el embarazo se debe comprobar si la infección ha pasado al feto. Esto se realiza por una amniocentesis a partir de la 21 semana de gestación. Se realiza una técnica molecular para detectar la presencia de material genético del virus en el líquido amniótico (PCR). Una PCR positiva indica infección del feto y una PCR negativa la hace improbable (aunque siempre hay que estudiar al niño al nacimiento).
En las mujeres con infección fetal demostrada (PCR positiva en líquido amniótico) debe hacerse un seguimiento ecográfico muy estrecho. En algunos centros administran tratamientos con gammaglobulina (defensas frente al virus) o antivirales para que la gravedad de la infección sea menor.
Las mujeres con PCR positiva en líquido amniótico darán a luz niños sin síntomas en un 85% de los casos. Solo el 15% de los recién nacidos tendrán síntomas, que pueden ir desde petequias o afectación hepática transitoria hasta sordera o daño neurólogico.
Al recién nacido deben hacerse pruebas microbiológicas para comprobar si ha contraído la infección, que consisten en una PCR para el virus en orina o saliva al nacer. Si esta prueba es positiva se confirma que el niño está infectado y deben realizarse pruebas adicionales para confirmar la extensión de la infección: analítica, ecografía cerebral, fondo de ojo, potenciales evocados auditivos y otras que considere el especialista.
Los niños que tienen alguna alteración en estas pruebas se consideran sintomáticos y tienen más riesgo de secuelas. La principal secuela es la sordera neurosensorial (40-50% de los casos), que puede aparecer al nacimiento o en los meses o años siguientes. Hay tratamientos frente al virus (ganciclovir intravenoso o valganciclovir oral) que disminuyen la posibilidad de que aparezca la sordera o que aumente si ya está presente al nacimiento. Estos tratamientos pueden bajar las defensas, por lo que los niños que los reciban deben hacerse analíticas seriadas para controlarles.
La principal secuela es la sordera neurosensorial (40-50% de los casos), que puede aparecer al nacimiento o en los meses o años siguientes.
Afortunadamente la posibilidad de problemas neurológicos importantes es poco frecuente, y solo suele aparecer en niños con la cabeza pequeña (microcefalia) o si tienen alteraciones importantes en la ecografía cerebral. Estos niños deben iniciar cuanto antes un tratamiento con fisioterapia y rehabilitación. Todos los niños sintomáticos deben hacer un seguimiento en consultas de pediatría/enfermedades infecciosas, otorrinolaringología, oftalmología y neurología.
Si los niños están infectados (orina o saliva positiva) pero todas las demás pruebas son normales, se consideran asintomáticos. En estos casos, hay mayor posibilidad que en la población general de que se desarrolle pérdida auditiva, pero tan solo en un 7%, por lo que no está indicado un tratamiento frente al virus, pero si un seguimiento por parte del otorrinolaringólogo.

